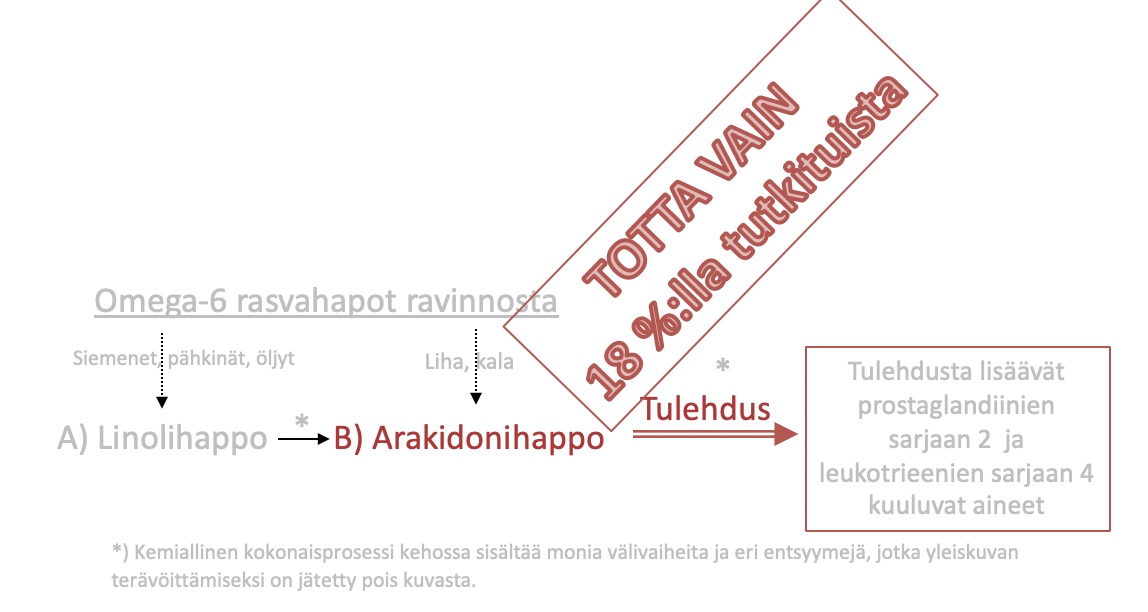
Varsin monilla ravintoasioista kiinnostuneilla on pitkään ollut vankka käsitys, että omega-6 rasvahapot lisäävät matala-asteista eli lievää tulehdusta. Tämän ajatuksen perusta juontaa pitkälti biokemian oppikirjojen ja netin kaavioihin, ilman perehtyneisyyttä ihmisillä tehtyihin viimeisen vuosikymmenen tutkimuksiin. Lyhyt kertaus vanhasta omega-6 rasvahappojen ja tulehduksen teoriasta: linolihappo muuttuu elimistössä arakidonihapoksi, joka aiheuttaa tulehdusta aiheuttavien aineiden lisääntymisen kehossa.
Olen kirjoittanut omega-6 rasvahappojen laajemmista terveysvaikutuksesta uusimmassa kirjassani Taltuta lievä tulehdus ja useaan kertaan blogissani, muun muassa täällä:
Linolihappo, rypsiöljy, Crohnin tauti ja haavainen koliitti
Ravinnon rasva ja matala-asteinen tulehdus (osa 2)
Omega-6 linolihappo, pieni paholainen vai pelastaja?
Noissa mainituissa kirjoituksissani olen osoittanut, että omega-6 rasvahappojen väitetyt tulehdusta lisäävät vaikutukset ovat pitkälti vanhentunutta tietoa, nykyään voisi puhua jopa harhauskosta. Lisäksi omega-6 rasvahapot vähentävät LDL-kolesterolia, apolipoproteiini B:tä ja verensokeria korvatessaan tyydyttynyttä rasvaa tai (raffinoitua) hiilihydraattia. Tämän vuoksi saksanpähkinää, rypsiöljyä ja margariinia on voinut syödä sinänsä huoletta pelkäämättä lievää tulehdusta näiden omega-6 rasvahappojen vuoksi.
Tiivistän aihetta koskevan monimutkaisen aiemman tieteellisen näytön eli tutkitun tiedon asiasta oheen:
1: Linolihapon runsas saanti (jopa 6-kertaiseksi lisääminen) ei lisää arakidonihapon määrää elimistössä, eikä 90 %:n vähentäminen vähennä arakidonihapon määrää lähtötilanteeseen nähden satunnaistettujen tutkimuksien systemoidun katsauksen mukaan (Rett & Whelan 2011). Tämä selittynee sillä, että minimaalinen määrä vain 0,3-0,6 % linolihaposta ylipäätään muuntuu arakidonihapoksi elimistössä (Demmelmeir 1999) ja sillä, että monissa ruuissa, erityisesti lihassa ja kalassa, on luontaista arakidonihappoa suurempia määriä kuin mitä linolihaposta keskimäärin muuntuu arakidonihapoksi elimistössä. On myös ilmeistä, että arakidonihappopitoisuus on tarkoin säädelty elimistössä.
2: Satunnaistetuissa tutkimuksissa omega-6 rasvahappojen, erityisesti linolihapon, erittäin runsas saanti ei lisää tulehdusta, eikä vähäinen saanti vähennä tulehdusta (Johnson & Fritsche 2011 ). Linolihapon saanti ollut tässä systemoidussa katsauksessa mukana olleissa lisäystutkimuksissa noin 2-5-kertainen suomalaiseen saantiin nähden eli 20-50 g/pv vs. 10 g/pv, kun taas vähennystutkimuksissa linolihapon saanti ollut n. 5 g/pv eli puolet siitä mitä keskimääräinen suomalainen saa.
3: Linolihapon runsas saanti ei ole yhteydessä CRP-tulehdusarvoon väestötutkimuksien meta-analyysissä (Su 2017)
4: Satunnaistetuissa tutkimuksissa arakidonihapon (todellinen uumoiltu ”pahis”), erittäin runsas saanti (3-kertaisesti suomalaiseen saantiin nähden) ei lisää tulehdusta ja vähäinen saanti (alle 30 % suomalaisesta keskimääräisestä saannista) ei vähennä tulehdusta (Calder et al. 2019 )
Nämä ovat vakuuttavia tutkimusaineistoja, joiden mukaan omega-6 rasvahapoilla ei ole keskimäärin tulehdusta lisäävää vaikutusta, ne ovat neutraaleja tai korvatessaan esimerkiksi tyydyttynyttä rasvaa jopa tulehdusta vähentäviä. Mutta voisiko tulehduksen synnyssä kuitenkin olla merkittävää yksilöllistä vaihtelua, vaikka keskimäärin mitään ei tapahtuisikaan omega-6 rasvojen saannin muuttuessa?
Uudet Itä-Suomen yliopiston uraauurtavat tutkimukset
Itä-Suomen yliopiston tutkijat Maria Lankisen johdolla ovat penkoneet asiaa uraa uurtavalla tavalla ensimmäisenä maailmassa. Lankinen ja tutkijakollegat ovat kiinnostuneita siitä, onko olemassa herkkiä ihmisjoukkoja, joilla omega-6 rasvahapot kuitenkin lisäävät tulehdusta. Edelleen heitä kiinnostaa se, onko olemassa henkilöitä, joilla omega-6 rasvahapot vähentävät tulehdusta. Tutkimus löytyy täältä.
Tutkimukselle pohjan loi tieto, että linolihappoa arakidonihapoksi muuntavassa elimistön reaktioketjussa viimeinen entsyymi on nimeltään delta-5-desaturaasi. FADS1-geeni puolestaan säätelee (”koodaa”) tuon delta-5-desaturaasi-entsyymin toimintaa. FADS tulee sanoista Fatty Acid DeSaturase, ja niinpä tuota delta-5-desaturaasi-entsyymiä näkee myös kutsuttavan, joskin varsin harvoin, fatty acid desaturase 1:ksi.
FADS1-geenistä löytyy erilaisia variantteja. Tässä tutkimuksessa keskityttiin yhteen vahvasti rasvahappoaineenvaihduntaa säätelevään varianttiin, josta esiintyy ihmisillä kolmea eri typpiä. Tyypit ovat TT, TC tai CC.
TT kuvaa sitä, että delta-5-desaturaasi-entsyymiä muodostuu elimistössä paljon. CC puolestaan sitä, että samaa entsyymiä muodostuu vain vähän. TC-geenin toiminta on välimuoto. Leikkisäksi muistisäännöksi voisi sanoa vaikka TT:n vastaavan Tehokkaasti Toimivaa entsyymiä nimittäin ne, joilla on TT -alleeli, delta-5-desaturaasi-entsyymia on paljon aiheuttaen tehokkaan reaktioketjun ”virrassa alaspäin”, ja siten erittäin runsaan arakidonihapon muodostuksen.
CC voisi puolestaan olla Curkeampaan Cuoritukseen kallellaan oleva geeni, sillä heillä ko. geenin koodaamaa entsyymiä syntyy vain vähän. TC-geenityypin omaavilla entsyymin muodostuminen on keskimääräistä.
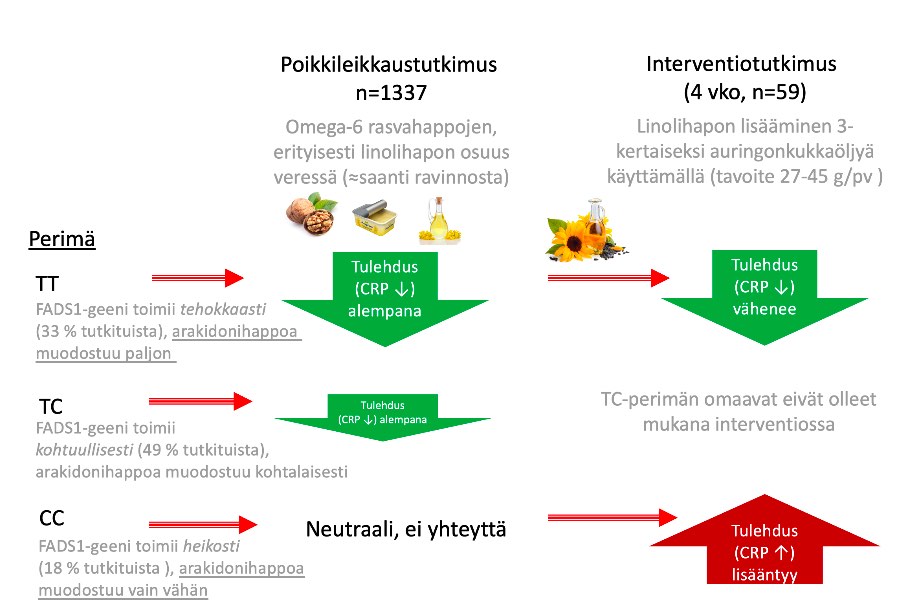
Ensimmäisessä väestön poikkileikkaustutkimuksessa (n=1337) tutkijat havaitsivat, että runsaampi linolihapon osuus veressä oli yhteydessä pienempään CRP-tulehdusarvoon erityisesti FADS1-geenin TT-genotyypillä. Näitä henkilöitä oli 33 % kaikista tutkituista itä-suomalaisista miehistä, naisia ei ollut mukana tässä METSIM-kohortissa. Suuri osa (49 %) tutkituista oli TC-alleelin omaavaa tyyppiä, ja heilläkin runsaampi linolihapon osuus veressä oli yhteydessä hieman pienempään CRP-arvoon.
Toisin sanoen, valtaenemmistö, eli 82 % tutkituista reilusta 1300 miehestä, oli sellaisia, joilla linolihapon kohonnut osuus veressä yhdistyi pienempään lievän tulehduksen mittariin eli herkällä menetelmällä mitattuun CRP:hen.
18 % tutkituista miehistä oli sellaisia, joilla FADS1-geeni oli muotoa CC. Näillä henkilöillä suurempi linolihapon osuus veressä ei ollut yhteydessä CRP-pitoisuuteen eli lievään tulehdukseen.
Tulokset ovat täysin päinvastoin perinteistä teoriaa, jonka mukaan suurempi linolihapon saanti, ja sitä myötä pitoisuus veressä, johtaa arakidonihapon määrän, ja siten tulehduksen lisääntymiseen. Voidaan siis sanoa, että juuri päinvastoin kuin aiemmin on kuviteltu, linolihapon lisääntynyt muuttuminen arakidonihapoksi (TT-tyypit) vähentää tulehdusta CRP:llä mitattuna. Tämä on iso uutinen.
Tutkijaryhmä päätti varmistaa tulokset satunnaistetulla tutkimuksella, onhan väestötutkimukset aina satunnaistettuja tutkimuksia alttiimpia virhelähteille.
He tekivät 59 koehenkilöä kattavan, 4 viikon interventiotutkimuksen auringonkukkaöljyllä, jossa on omega-6 rasvahappoja kolme kertaa enemmän kuin Suomessa eniten kulutettavassa öljyssä, rypsiöljyssä.
Tutkimuksessa jokainen koehenkilö söi auringonkukkaöljyä 27–45 g/pv riippuen koehenkilön painosta, ja linolihapon saanti nousi tavanomaiselta suomalaiselta tasolta 10 g/pv tasolle 31 g/pv. Linolihapon saanti kasvoi siis huimat 200 % miesten ”kotioloihin” nähden. Mukaan otettiin vain homotsygoottisia geenityyppejä eli ääripäitä TT ja CC, joiden oletettiin reagoivan eniten linolihapon saannin lisääntymiseen edellisen poikkileikkaustutkimuksen pohjalta. TC-tyypit (heitä oli alunperin 49 % kaikista) suljettiin pois.
Tulokset ovat yhdensuuntaisia poikkileikkaustutkimuksen kanssa. Kun vanhan opin mukaan kaikkien pitäisi pamahtaa tukevasti tulehduksen puolelle niin nyt kävikin niin, että TT-genotyypin omaavilla tulehdus väheni lähtötilanteeseen nähden. Aktiivisesta delta-5-desatuuraasista ja hyvin runsaasta linolihapon saannista huolimatta, myöskään arakidonihapon elimistössä pitoisuus ei noussut. Sen sijaan CC-genotyypillä näytti käyvän niin, että tulehdus oli lisääntymään päin, vaikka heillä arakidonihapon pitoisuus jopa laski merkittävästi.
Tulokset kaikkinensa ovat myös samansuuntaisia kuin Jyrki Virtasen vetämän tutkimusryhmän tulokset (2018) Kuopiosta; linolihapon runsas saanti oli yhteydessä pienempään CRP-arvoon etenevässä KIHD-kohortissa. Margariini oli tässä aineistossa tärkein omega-6 rasvahappojen lähde.
Kiinnostava kysymys on, miksi tulehdus ei lisäännykään elimistössä, vaikka arakidonihappoa syntyy vilkkaammin linolihaposta. Tähän ei ole selvää selitystä tutkijoillakaan. Itse pidän mahdollisena, että arakidonihapon aineenvaihdunnassa syntyvät tulehdusta vähentävät lipoksiini A4 (LXA4) ja epoksieikosatrienihapot (EET:t), johtavat tulehdusreaktioiden vähenemiseen (Das 2018).
”Studies showed that AA [arachidonic acid] and its metabolites especially, lipoxin A4 (LXA4) and epoxyeicosatrienoic acids (EETs), potent anti-inflammatory metabolites, have a crucial role in the pathobiology of hypertension and diabetes mellitus. AA, LXA4 and EETs regulate smooth muscle function and proliferation, voltage gated ion channels, cell membrane fluidity, membrane receptors, G-coupled receptors, PPARs, free radical generation, nitric oxide formation, inflammation, and immune responses that, in turn, participate in the regulation blood pressure and pathogenesis of diabetes mellitus”
–Undurti Das 2018
Lopuksi
Kuopiolaisen tutkimusryhmän tulokset ovat monella tapaa merkittäviä. Ne muun muassa kannustavat tutkimaan lisää erilaisia geenien ja ravintotekijöiden yhteisvaikutuksia. Yksilölliset vasteet saattavat joskus hukkua keskiarvojen vertailuihin.
Tällaisten tutkimusten pohjalta voimme ehkä myöhemmin siirtyä yksilöllisemmin ruokavalioneuvontaan, ja siten saada entistä parempia tuloksia aikaan elintapamuutoksin. Valitettavasti vielä emme ole FADS1-geenin(kään) osalta perillä tällaisessa tilanteessa. Tutkijat itse päättelevät:
”It remains to be elucidated if it would be beneficial to have genotype-based modifications in recommendations for the intake of LA [linoleic acid] and possibly also for n–3 fatty acids.”
Tulokset myös tekevät harvinaisella tavalla läpinäkyväksi sen, miten koeputkessa, muissa kokeellisissa malleissa tai loogisen päättelyn pohjalta syntyneet teoriat voivat olla ydinsanomaltaan vääriä –teoriat pitää tutkia ihmisillä kunnollisin menetelmin. Hyvin runsaskaan linolihapon saanti ei nosta arakidonihapon pitoisuutta eikä tulehdusta edes niillä henkilöillä, joilla linolihapon metaboloituminen arakidonihapoksi on erityisen vilkasta.
Arakidonihapon osuus tulehduksissa on syytä arvioida täysin uusiksi, viittaan kuopiolaistutkimuksen lisäksi kirjoituksen alussa esitettyihin meta-analyyseihin ja siihen, että arakidonihapon saanti nostamalla korkealle on havaittu joitain alustavia myönteisiä vaikutuksia lihaskasvuun ja muistiin (Calder et al. 2019 )
Yhdessä tämän kirjoituksen alussa referoitujen tutkimuksien kanssa kuopiolaistutkimukset vahvasti viittaavat siihen suuntaan, että vallalla ollut teoria omega-6 rasvahappojen väitetystä tulehdusta lisäävästä vaikutuksesta on totta vain vähemmistöllä, noin joka viidennellä meistä. Juuri päinvastoin kuin samainen teoria on esittänyt, omega-6 rasvahapot vähentävät tulehdusta ainakin joka kolmannella meistä –loppujenn meistä, eli TC-geenityyppien osalta omega-6:t ovat tulehduksen osalta joko neutraaleja tai tulehdusta vähentäviä.
Sille pienehkölle osalle väestöä (1/5), jolle omega-6 rasvahapot saattavat aiheuttaa lisääntynyttä tulehdustaipumusta, ne vastapainoksi vähentävät apolipoproteiini B:tä, LDL-kolesterolia ja verensokeria kuten kuopiolaisten poikkileikkaustutkimuskin osoitti –jopa tällä CC-porukalla omega-6 rasvahappojen vaikutus voi siis olla hyvinkin nettopositiivinen kokonaisterveyttä ajatellen. Tulehdushan on vain yksi riskitekijä tunnettujen muiden, kuten verenpaine, LDL-kolesteroli, apolipoproteiini B, verensokeri, joukossa, ei mitenkään niitä ylempänä.
Suurimmalle osalle meistä, 82 %:lle ehkä, omega-6 rasvahappojen runsas saanti ravinnosta, aiheuttaa suuren nettopositiivisen hyödyn, edellä mainituista syistä johtuen.
Voidaan kuitenkin spekuloida, mutta vain spekuloida tässä vaiheessa, olisiko mahdollista että FADS1- geenin CC-tyypin omaavat henkilöt olisivat myös alttiimpia sairauksille, joissa tulehduksella on iso rooli. Kuopiolaistutkimus toiminee kimmokkeena asian selvittämiselle tulevaisuudessa.
Kuten aina tieteellistä näyttöä tulkittaessa, on tässäkin hyvä jättää ovi auki jatkotutkimuksille. Kuopiolaisten tulokset on tarpeen saada toistettua lisätutkimuksissa. Kyseessä oleva tutkimus ei ole vielä piste tälle tarinalle.
Lankinen MA, Fauland A, Shimizu B-i, Agren J, Wheelock CE, Laakso M, Schwab U, J. Inflammatory response to dietary linoleic acid depends on FADS1 genotype. Am J Clin Nutr. 2019;109(1):165–175.
Laajemmin ruokavalion ja ravintolisien vaikutuksista tulehduksiin voit lukea esimerkiksi 2019 julkaistussa kirjassani Taltuta lievä tulehdus